近日,深圳市第二人民医院(深圳大学附属第一医院)神经外科正式启动了Vorasidenib桥接临床试验。Vorasidenib是一款高活性、口服、能穿透血脑屏障的IDH1/IDH2双靶点抑制剂,可抑制突变的IDH1和IDH2蛋白,该产品由施维雅(Servier)在2020年收购Agios所得。
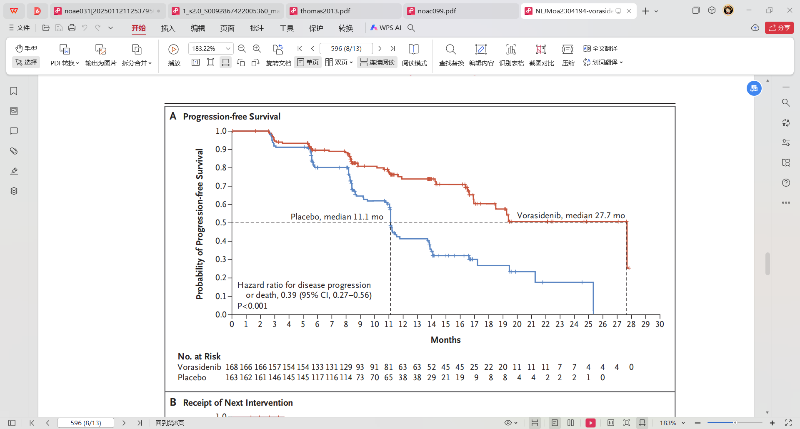
2023年8月在新英格兰杂志(NEJM)发表的三期临床研究文章显示,Vorasidenib能够延长低级别胶质瘤(IDH突变型,WHO2级)患者无进展生存期(PFS),PFS为27.7个月,而安慰剂组为11.1个月,PFS风险比为0.39(95%
CI:0.27,
0.56),p<0.0001。此外,vorasidenib组中位TTNI未达到,安慰剂组的中位TTNI为17.8个月(HR=0.26;95%
CI:[0.15,
0.43],p<0.0001)。也正是基于这个研究结果,2024年8月6日,美国FDA批准了Vorasidenib上市(商品名为Voranigo),用于12岁及以上伴有易感IDH1或IDH2突变的2级少突胶质细胞瘤或星形细胞瘤儿童和成人患者,这些患者此前接受过手术包括活检、次全切或全切。
为探索Vorasidenib在亚洲低级别胶质瘤患者中的有效性,由北京天坛医院神经外科江涛院士领衔,将在北京天坛医院、上海华山医院和深圳市第二人民医院(深圳大学附属第一医院)等全国15家中心开展Vorasidenib桥接临床试验。2024年8月31日,Vorasidenib桥接临床试验在北京正式启动。


项目启动后,3家分中心顺利完成了安全导入期研究,确认Vorasidenib在中国低级别胶质瘤患者的安全性后,项目组于2025年1月20日宣布可以开展随机双盲阶段。2025年1月22日上午9点,深圳市第二人民医院(深圳大学附属第一医院)神经外科黄国栋主任作为分中心PI主持了该项目在我院的启动会,项目启动后我院是继北京天坛医院、上海华山医院等分中心后全国第6家、华南地区首家正式开展该项目的医院。
参加本次项目启动会的有神经外科、GCP项目机构办、影像科、病理科的专家教授,启动会上黄国栋主任向参会人员介绍了低级别胶质瘤的治疗现状:对于复发低级别胶质瘤主要的治疗方式有手术、放疗和化疗,化疗以传统化疗药为主,因为担心放化疗的副反应及低级别胶质瘤的良好预后,欧洲、美国及国内专家对手术后放化疗方案及治疗时机持有不同观点。新英格兰杂志的研究证明Vorasidenib能延长低级别胶质瘤患者接受放化疗的时间,延缓放化疗给患者带来的认知功能障碍。但Vorasidenib在中国低级别胶质瘤患者中是否同样有效,需要研究证实,这也是本研究的目的。本研究的入排标准中,有一条尤其值得大家关注——“排除手术或活检后未接受任何抗癌治疗,包括全身化疗、放疗、疫苗、小分子、IDH抑制剂、研究药物等”,极为严格。希望各位研究者严格遵照中国GCP相关制度、医疗规章制度及研究者手册实施本研究。另外,被分到安慰机组的患者在肿瘤进展、揭盲后可以继续服用Vorasidenib,这是本研究的项目组考虑得比较周全,给对照组的患者提供了一个治疗选择。最后,希望通过我们的努力能给中国低级别胶质瘤患者带来福音。

供稿:邓忠、黄国栋
审核:健康宣教科
发布:医院办公室